Molte coppie che vogliono partecipare al programma di trattamento per l’infertilità sono interessati ai dettagli del FIVET, come si fa e come prepararsi correttamente per la procedura.
Prima di iniziare il tratamento, la coppia si sottopouone a esami medici e tutte le prove necessarie. Le madri future sono sottoposte ad un controllo ginecologico, ultrasuoni, analisi delle malattie infettive e dei livelli ormonali. Gli uomini fanno uno spermogramma e i test per l’infezione. A questo punto la causa dell’infertilità è spesso chiara e viene scelta la procedura IVF più appropriata.
Le fasi principali della fecondazione in vitro:
- Stimolazione ovarica
- Prelievo ovocitario e pretrattamento del liquido seminale
- Fecondazione : FIVET o ICSI
- Coltura in vitro degli embrioni
- Trasferimento degli embrioni in utero (embryo transfer)
- Sostegno luteale
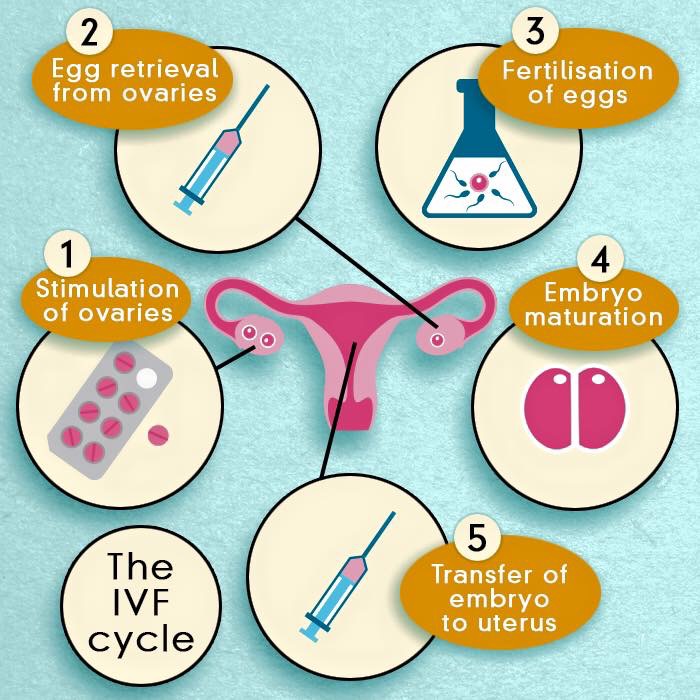
Foto: Le fasi della FIVET
In genere si utilizzano farmaci che stimolano una maggiore produzione di ovuli (tra 10 e 12 ovuli), vale a dire che si persegue la cosiddetta superovulazione, per avere maggiori possibilità. Questa fase viene controllata tramite ecografie transvaginali e determinazioni dell’estradiolo nel sangue. Quando si reputa che i follicoli sono maturi (tra 16-18 mm di diametro), si programma l’estrazione degli ovuli.
Il protocollo di stimolazione si definirà in modo personalizzato a seconda della riserva ovarica della paziente.
Nella maggior parte dei casi saranno sufficienti tre controlli ecografici per poter programmare il pick-up degli ovociti. Gli stessi possono essere realizzati qui in Clinica oppure in Italia.
Una volta ottenuta la maturazione dei follicoli, si procede ad aspirarli per ottenere gli ovuli. Questa operazione viene effettuata tramite agoaspirazione ovarica controllata mediante ecografia in sala operatoria, con una leggera sedazione. L’intervento dura in genere 15 minuti e la paziente, di solito, torna a casa 2 ore dopo lo stesso. Il liquido follicolare prelevato viene mandato al laboratorio dove, con il microscopio, si individuano gli ovuli e si effettua una stima della loro qualità e la maturità.
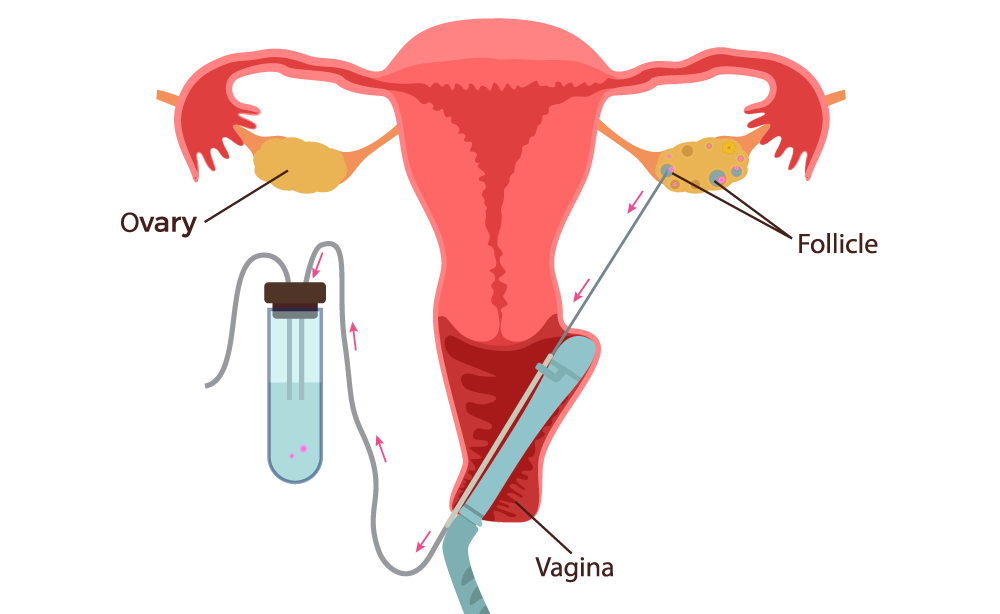
Foto: Il Prelievo degli ovuli
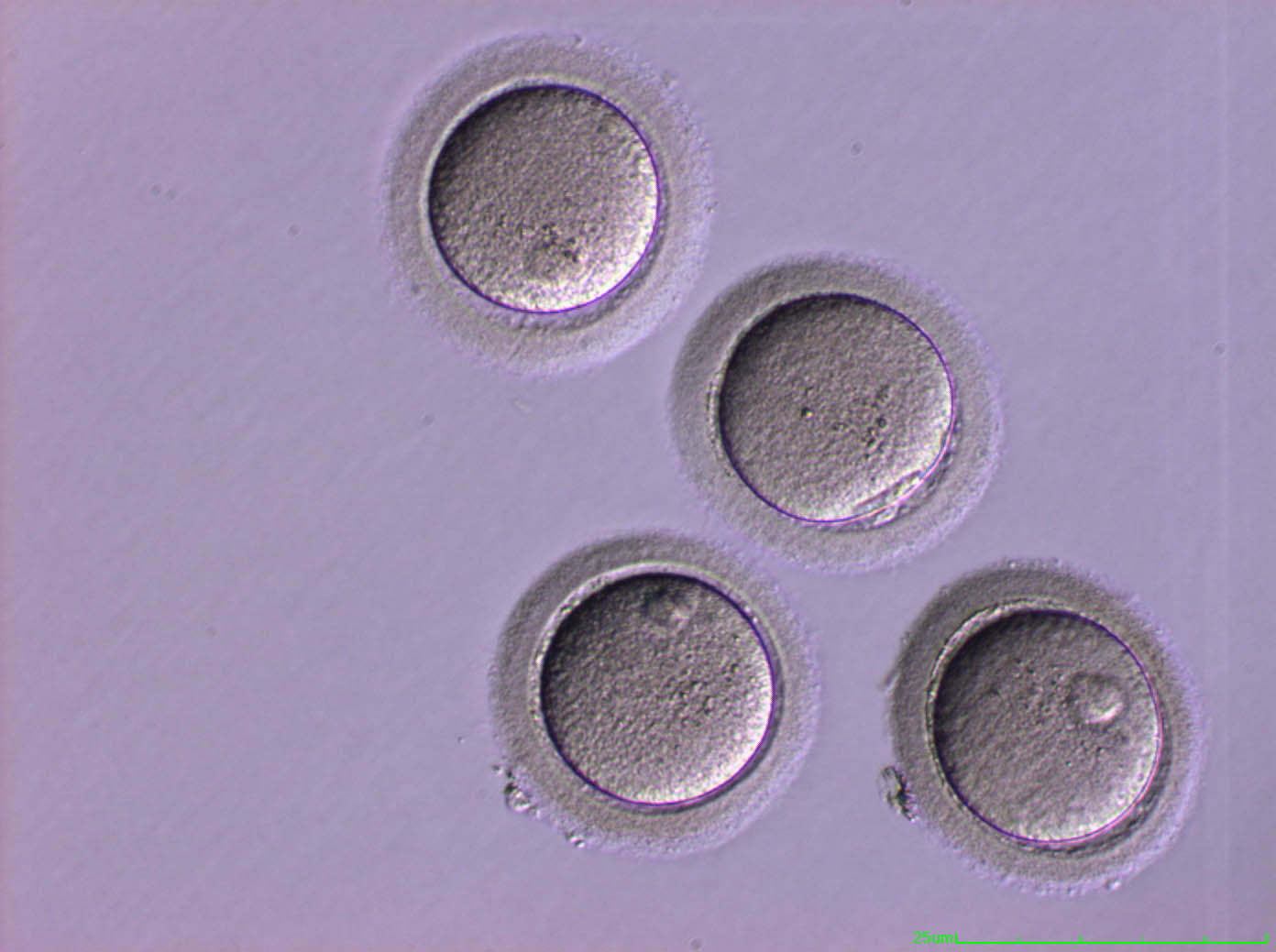
Foto: Ovociti maturi (American Hospital Tirana)
Presso il nostro centro, gli embrioni possono essere coltivati fino al 5°/6° giorno , fino lo stadio di blastocisti. La valutazione dello sviluppo embrionale nel nostro centro viene effettuata attraverso sophisticate apparechiature di ultima generazione. La valutazione embrionale si basa sullo sviluppo morfologico, sul numero delle cellule e sulla frammentazione citoplasmatica dell’embrione.
- Giorno 0: giorno in cui viene eseguito il pick-up ovocitario, la raccolta del liquido seminale e l’inseminazione degli ovociti.
- Giorno 1: il primo giorno, precisamente dopo 16-18 ore dall’inseminazione, viene effettuato il controllo della fertilizzazione. Sono fertilizzati gli zigoti che presentano i due pronuclei, uno di origine materna e uno di origine paterna.
- Giorno 3: controllo dopo circa 72 ore dall’inseminazione. Generalmente gli embrioni in questo stadio sono costituiti da un numero di cellule ≥ 7.
- Giorno 5: controllo dopo circa 120 ore dall’inseminazione. Gli embrioni in questa fase sono allo stadio di blastocisti, condizione caratterizzata dalla presenza di due tipi di cellule differenziate. Le cellule del trofoblasto, che daranno origine alla placenta, e le cellule dell’embrioblasto, che daranno origine al feto. In genere a questo stadio viene effettuato l’embrio-transfer. Il 5° giorno dopo la fecondazione degli ovociti: l’esame PGD/PGS, embriotransfer, la possibilità di congelare gli embrioni di buona qualità.
- Giorno 6: controllo dopo circa 144 ore dall’inseminazione. In questa fase di sviluppo, tutti gli embrioni dovrebbero trovarsi allo stadio di Blastocisti. In questo giorno può essere effettuato l’embriotransfer e/o la crioconservazione, se non sono stati eseguiti il giorno precedente.
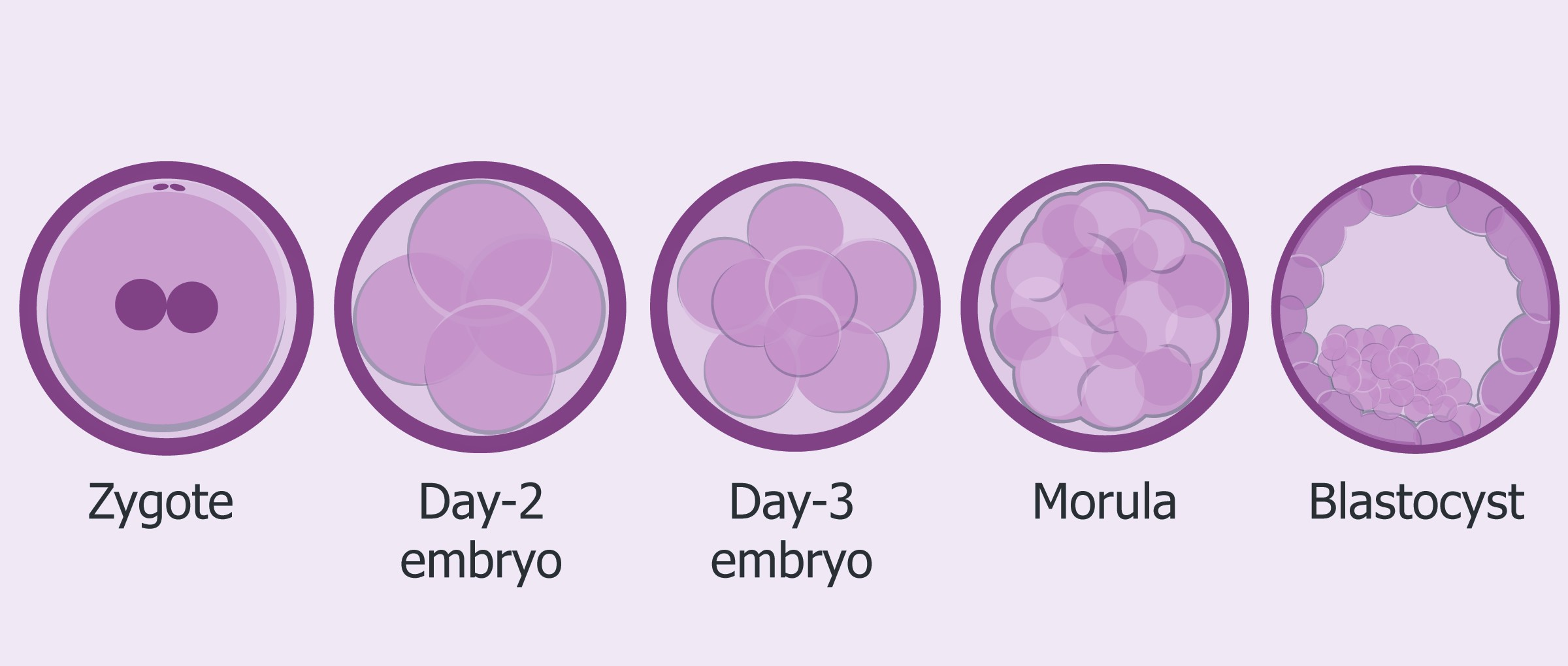
Foto: Sviluppo del emrbrione
Il 5° o 6° giorno dopo la fecondazione degli ovociti è possibile eseguire:
- La PGD / PGS, nel caso in cui si ritenga necessario effettuare lo studio genetico degli embrioni;
- l’embriotransfer (a meno che non sia stato fatto il quinto giorno);
- ilcongelamento degli embrioni sovrannumerari di buona qualità.
Assited Hatching
Cosa è l’Hatching assistito?
Durante le prime fasi di sviluppo l’embrione è protetto da uno strato esterno definito “zona pellucida”, dal quale si libera per stabilire un contatto con le cellule dell’utero. Questo processo di schiusa è denominato, in inglese, “Hatching” ed è di fondamentale importanza perché consente l’impianto dell’embrione in utero. La mancata fuoriuscita di un embrione dalla membrana è, quindi, uno dei motivi del mancato esito di una gravidanza.
L’ hatching assistito è una tecnica di micromanipolazione degli embrioni. L’ hatching assistito è un procedimento che prevede di praticare un foro nella zona pellucida, involucro che circonda l’embrione, in fase di sviluppo. Tale tecnica viene eseguita con un particolare raggio laser che ne consente il naturale processo di schiusa. Viene praticato sull’embrione al terzo giorno di sviluppo e non crea alcun danno allo stesso. Questa tecnica può determinare la riuscita di un trattamento di Procreazione Medicalmente Assistita, FIVET o ICSI, aiutando l’impianto dell’embrione nella parete uterina. Questa tecnica aiuta l’embrione a fuoriuscire dal suo involucro creando delle condizioni favorevoli per:
- poter effettuare la biopsia e la diagnosi preimpianto allo stadio di blastocisti;
- favorire l’annidamento dell’embrione nell’utero.
Quando puo essere effetuato l’hatching assistito?
L’hatching assistito viene effettuato al terzo giorno della coltivazione, quando l’embrione è costituito da 7-10 cellule.
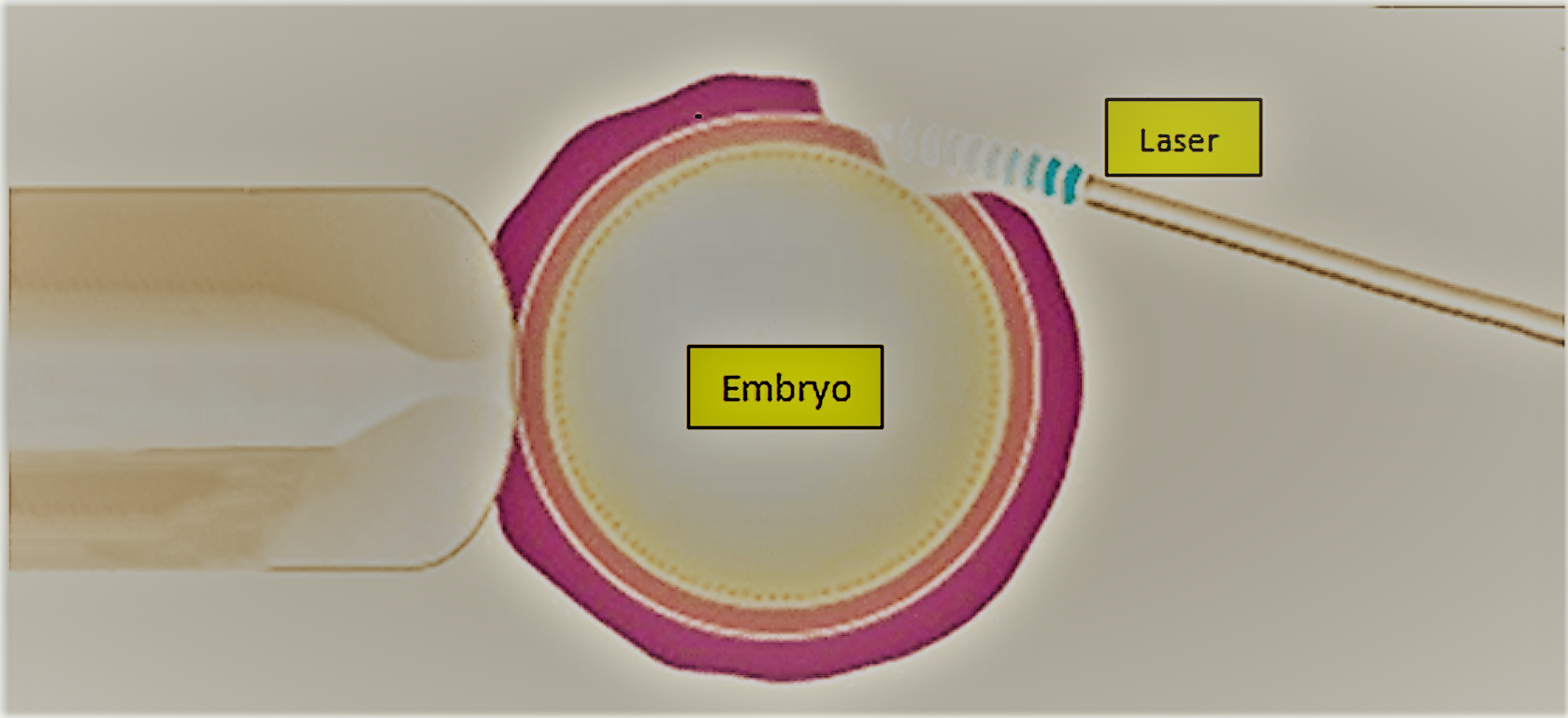
Foto: Assisted hatching
In quali casi è opportuno eseguire l’hatching assistito?
L’indicazione fondamentale a questa procudura è costituita da embrioni che hanno la zona pellucida troppo spessa, il che potrebbe bloccare la fuoriuscita delle cellule e l’impianto dell’ embrione nell’utero.
Ogni qualvolta viene effettuata la Diagnosi Preimpianto (PGD/PGS) è necessario eseguire l’Hatching Assistito per poter effettuare un microforo dal quale prelevare un campione di cellule embronali.
Altre indicazioni per l’hatching assistito:
- Nelle donne più mature che presentano ovociti con una pellicola più dura.
- Nei casi di fallimento ripetuto dell’impianto.
- Prima del trasferimento di embrioni crioconservati.
- Per eseguire la diagnosi genetica preimpianto.
Diagnosi Genetica Preimpianto (PGD / PGS)
Che cos’e’ la PGD?
L’evoluzione delle tecniche di fertilizzazione in vitro e la possibilità di ottenere cellule gametiche ed embrionali utilizzabili per la diagnosi di patologie genetiche, ha determinato un ampliamento delle prospettive della diagnosi prenatale, consentendo di trasferire l'epoca della diagnosi dalla fase 'post-impianto' a quella 'pre-impianto'.
La Diagnosi Genetica Preimpianto (PGD) permette di identificare la presenza di malattie genetiche o di alterazioni cromosomiche su ovociti e/o embrioni ottenuti durante un ciclo di fertilizzazione in vitro prima del loro trasferimento in utero. La procedura consiste nell’analizzare una singola cellula dell'embrione al fine di trasferire solo embrioni risultati normali all’analisi.
La PGD, quindi, permette di realizzare un importante traguardo, che è quello evitare il ricorso all’aborto terapeutico, spesso devastante dal punto di vista psicologico e non sempre accettato dal punto di vista etico/morale.
Come avviene?
Una volta che si è ottenuta la fertilizzazione, si prelevano dagli embrioni ai primi stadi di sviluppo una o due cellule (blastomeri), il cui DNA sarà analizzato in relazione al tipo di malattia genetica che si vuole diagnosticare. Gli embrioni che risulteranno non affetti dalla patologia genetica, si potranno dunque trasferire in utero ed ottenere così una gravidanza senza la specifica malattia.
L’esecuzione della diagnosi genetica preimpianto si articola in differenti fasi che richiedono una stretta coordinazione tra due diverse equipe: i team del centro di procreazione medicalmente assistita (PMA) e del laboratorio di genetica molecolare. Ecco in sintesi le fasi:
- Fase 1. Stimolazione della funzione ovarica
- Fase 2. Prelievo dei gameti e fecondazione:
-
- Prelievo degli ovociti (pick-up)
- Iniezione intracitoplasmatica dello spermatozoo (ICSI)
- Fase 3. Coltura in vitro degli embrioni
- Fase 4. Biopsia dell’embrione
- Fase 5 .Analisi genetica dei blastomeri
- Fase 6. Trasferimento degli embrioni in utero (embryo transfer)
- Fase 7. Accertamento della gravidanza
A chi si rivolge?
Come tutte le tecniche di PMA anche questa procedura è destinata alle coppie che soffrono di comprovata infertilità. Inoltre, questa tecnica è indicata e consentita solo per le coppie che presentano determinate condizioni amnestiche ovvero cosiddette “ad elevato rischio riproduttivo”, con malattie sessualmente trasmissibili.
Le patologie genetiche più comuni nella popolazione italiana, in cui la PGD oggi trova una valida applicazione comprendono: Beta-Talassemia, Anemia Falciforme, Emofilia A e B, Distrofia Muscolare di Duchenne-Becker, Distrofia Miotonica, Fibrosi Cistica, Atrofia Muscolare Spinale (SMA) e X-Fragile.
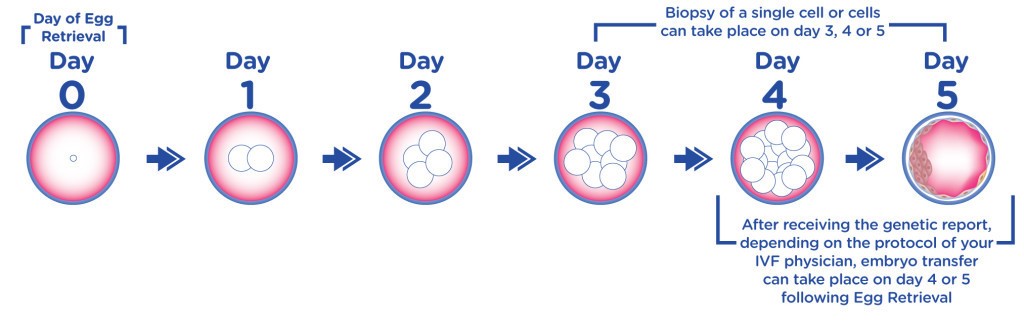
Foto: Diagnosi Genetica Preimpianto
Time lapse imaging - Embryoscope
Cos’è Embryoscope?
Embryoscope è un incubatore di embrioni di ultima generazione che incorpora una tecnologia di cattura delle immagini a intervalli di tempo prestabiliti (time-lapse). Permette di ottenere un video completo degli embrioni sin dall’inizio della loro vita e per tutto il tempo in cui rimangono sotto osservazione.
Che vantaggi offre Embryoscope?
Embryoscope migliora le condizioni di coltura degli embrioni rispetto agli incubatori convenzionali per cui aumenta le possibilità di ottenere una gravidanza. Ogni embrione, all’interno dell’Embryoscope, dispone di un proprio pozzetto individuale per cui non condivide il mezzo di coltura con gli altri embrioni. Il sistema di cattura delle immagini time-lapse consente il monitoraggio continuo degli embrioni in qualsiasi momento senza necessità di estrarli dall’incubatore per cui gli embrioni non subiscono alcuna alterazione dovuta a possibili cambi di temperatura o di luce. Al non esserci variazioni nelle condizioni di coltura, gli embrioni ottenuti sono quindi di migliore qualità e, pertanto, hanno maggiori possibilità di dar luogo a una gravidanza.
Il fatto di disporre di un sistema di registrazione continua dello sviluppo degli embrioni ci permette di determinare i ritmi di divisione cellulare ed in questo modo selezionare gli embrioni morfologicamente migliori nonché di individuare quelli che si sono divisi nel momento migliore. Mediante questa tecnica si possono selezionare gli embrioni con maggiori possibilità d’impianto e così ottenere le migliori probabilità di dar luogo a una gravidanza.
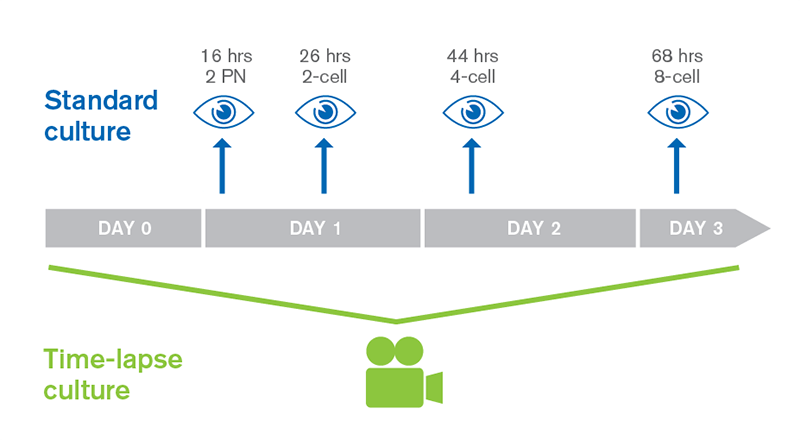
Foto: Time lapse imaging of the embryos
La valutazione degli embrioni.
Dopo la fecondazione le uova fecondate (gli embrioni) vengono regolarmente coltivate in laboratorio per 3-5 giorni prima di essere trasferite nell'utero della donna. Prima del trasferimento, gli embrioni sono valutati da un embriologo per selezionare gli embrioni con la migliore possibilità di impiantarsi nell'utero e formare un bambino sano.
Transfer embrionario.
Il numero di embrioni da trasferire viene stabilito in base a diversi parametri come la qualità embrionale, le caratteristiche e l'età della paziente, i tentativi precedenti di gestazione tramite FIVET, ecc. In generale si trasferiscono 1 o 2 embrioni e solo eccezionalmente se ne possono trasferire 3, il numero massimo previsto dalla legge. L'embrione o gli embrioni vengono trasferiti nell’utero mediante un sottile catetere e sotto supervisione ecografica. Il trasferimento risulta veloce ed indolore (senza anestesia) e la degenza è di circa 15-20 minuti. Nei successivi 3-4 giorni è consigliabile evitare sport e sforzi eccessivi.
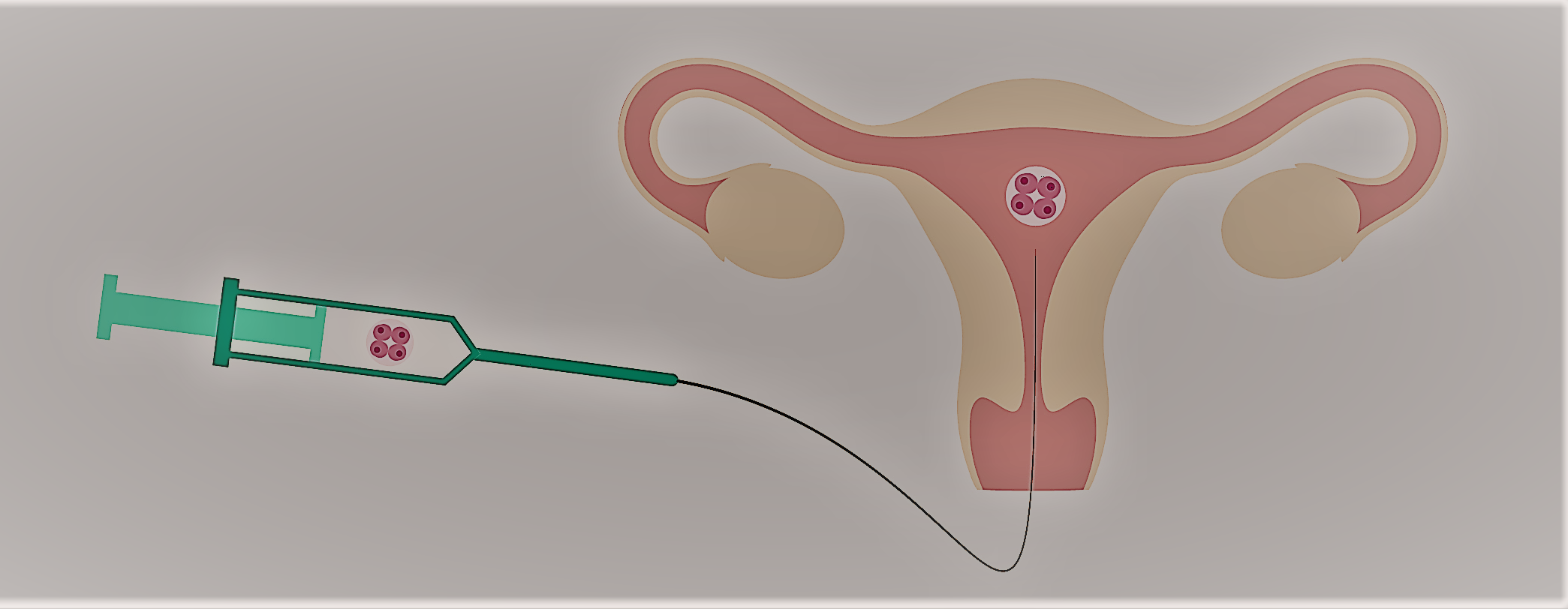
Foto: Embryo Tranfer
Le terapie di procreazione medica assistita comportano la necessità di sostenere la fase luteale, quella successiva, cioè, al prelievo degli ovociti e al trasferimento degli embrioni. Nei cicli stimolati, infatti, la fase luteale è certamente deficitaria e deve essere sostenuta farmacologicamente, al fine di garantire una condizione ottimale dell'endometrio a favorire l'impianto e lo sviluppo della gravidanza.
La fase luteale viene supportata dal giorno del prelievo degli ovociti con progesterone naturale intravaginale o intramuscolare.
Il supporto della fase luteale deve essere mantenuto sino al dosaggio delle bHCG che indica la presenza o assenza di un impianto ed, in caso di esito positivo, sino ad almeno 8 settimane di gestazione, venendo poi sospesa in modo graduale.
